12月11日,江西省药品监督管理局发布《江西省药品批发(连锁)企业量化分级分类监督管理办法(试行)》(以下简称《征求意见稿》)。
如有意见建议,请于2024年1月11日前以电子邮件方式发送至jxsypjyc@126.com,或将书面意见建议寄至南昌市北京东路1566号江西省药品监督管理局药品经营监督管理处。逾期视为无。
三个监管级别
《征求意见稿》指出,按照企业《药品经营许可证》经营范围由高到低分为三个监管级别:
一级监管是指:企业《药品经营许可证》经营范围中含有麻醉药品、第一、二类精神药品、药品类易制毒化学品、医疗用毒性药品、中药饮片(含毒性)、细胞治疗类血液制品、罂粟壳及疫苗储存配送企业;
二级监管是指:企业《药品经营许可证》经营范围中含有生物制品(含冷藏冷冻药品)、血液制品、蛋白同化制剂、肽类激素、体外诊断试剂(药品);
三级监管是指:企业《药品经营许可证》经营范围中含有中药饮片、中成药、化学药;
企业经营范围涉及多个监管级别的,按最高级别对其监管。企业变更经营范围的,按经营范围重新划定监管等级,但监管类别不变。
每一监管级别,从高到低分为三个监管类别。一类监管企业,为重点监管对象;二类监管企业,为主要监管对象;三类监管企业,为一般监管对象。各企业初始监管等级为第三类。
频繁变更许可,视为存在质量风险
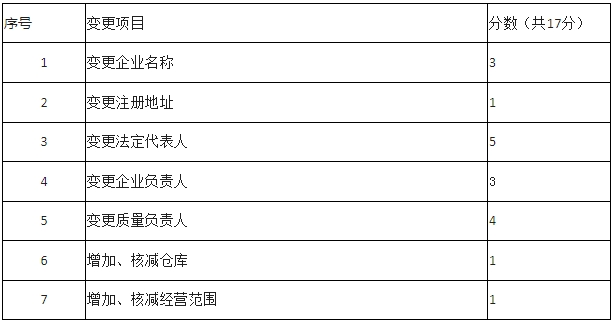
《征求意见稿》明确,企业《药品经营许可证》频繁变更,视为存在质量风险。省局按变更频次和项目量化分值,累计评分(变更项分值详见表格)并在省局网站公示。一次变更多个项目的,需累计分值。
企业质量安全风险分级每年评定一次。以当年度12月25日起往前追溯一年为一个评定年度。在评定年度5月31日后取得药品经营许可证的企业,不参加当年度评定,在此期间的评定信息计入下一评定年度。
企业质量安全风险分级评定根据本办法附件规定的分级指标开展,分为自评、信息核对、初评、结果告知和异议申请、异议处理和终评五个阶段。
分级分类动态监管
《征求意见稿》还指出,省药监局有关处室和直属单位应当加强对药品经营质量安全风险分级结果的综合运用,合理确定监管重点、监管措施和监管频次等。
企业年度质量安全风险分级积分初值为100分,每一年度内,企业积分降至80分时,在企业本年度及下一年度提高一个监管级别;降至60分至80分(不含)时,省局对企业负责人或法定代表人进行约谈,同时对企业本年度及下一年度提高一个监管类别和一个监管级别;低于60分时,该企业连续三年应被列为一级一类监管企业。
省局依据上述原则实施量化分级分类动态监管,并及时公布相关信息。
一类监管企业将被飞行检查
《征求意见稿》强调,省局有关处室、直属单位应当根据药品经营质量安全风险分级结果合理确定、动态调整常规检查频次,实施差异化分级监管,制定全省监督检查计划。
检查员中心、樟树药监局对企业按量化分级、分类信息,采取飞行检查、专项检查和日常检查、企业自查等多种手段强化监管。
检查员中心将对一级监管企业,每年不少于一次的监督检查;二级监管企业,对其每两年不少于一次的监督检查;三级监管企业,对其每三年不少于一次的监督检查。
一类监管企业将采取飞行检查的模式进行监管,二类监管企业将采取专项检查的模式进行监管,三类监管企业将采取日常检查或企业自查的模式进行监管。
企业处于歇业状态的,应及时主动报告,省局对企业状态予以公开。 来源:GSP办公室











